Octafil Low 200 IU/ml pulver och vätska till injektionsvätska, lösning
Human koagulationsfaktor VIII
Allmänna direktiv
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
- Spara denna information, du kan behöva läsa den igen.
- Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
- Detta läkemedel har ordinerats enbart åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar sjukdomstecken som liknar dina.
- Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt Eventuella biverkningar.
I denna bipacksedel finns information om följande
- Vad Octafil Low är och vad det används för
- Vad du behöver veta innan du använder Octafil Low
- Hur du använder Octafil Low
- Eventuella biverkningar
- Hur Octafil Low ska förvaras
- Förpackningens innehåll och övriga upplysningar
1. Vad produkten är och vad den används för
Octafil Low tillhör en läkemedelsgrupp som kallas koagulationsfaktorer och innehåller koagulationsfaktor VIII från humant blod. Detta är ett speciellt protein som gör att blodet koagulerar.
Octafil Low används för att behandla och förhindra blödning hos patienter med hemofili A. Detta är en sjukdom som gör att man blöder längre än vad man normalt skulle förvänta sig. Sjukdomen beror på en ärftlig brist på koagulationsfaktor VIII i blodet.
2. Vad du behöver veta innan produkten används
Det rekommenderas starkt att varje gång man får en dos Octafil Low, upptecknar preparatets namn och batchnummer för att upprätthålla en lista över använda satser.
Din läkare kan rekommendera att du överväger vaccinering mot hepatit A- och B-virus om du regelbundet eller upprepade gånger får humant faktor VIII produkter.
Använd inte Octafil Low
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du använder Octafil Low.
Octafil Low innehåller mycket små mängder av andra humana proteiner. Alla läkemedel som innehåller proteiner och som injiceras i en ven (intravenös administrering) kan ge upphov till allergiska reaktioner (se Eventuella biverkningar “Eventuella biverkningar”).
Utveckling av inhibitorer (antikroppar) är en känd komplikation som kan uppträda vid behandling med alla faktor VIII-läkemedel. Inhibitorerna hindrar, särskilt vid höga halter, att behandlingen fungerar som den ska. Du eller ditt barn kommer att övervakas noggrant avseende utveckling av sådana inhibitorer. Om du eller ditt barn drabbas av en blödning som inte kan kontrolleras med Octafil Low ska du omedelbart tala om det för din läkare.
Information om blod och plasma som används för framställning av Octafil Low
När läkemedel framställs av humant blod eller plasma vidtas speciella åtgärder för att förhindra att infektioner överförs till patienter. Detta inkluderar ett noggrant urval av blod- och plasmagivare för att säkerställa att personer med risk för att vara smittbärare utesluts, samt test av enskilda donationer och plasmapooler för tecken på virus/infektion. Tillverkarna av dessa produkter inkluderar dessutom steg i hanteringen av blod och plasma som kan inaktivera eller avskilja eventuella virus. Trots detta kan risken för överföring av infektion inte helt uteslutas när läkemedel tillverkade av humant blod eller plasma ges. Detta gäller även nya, hittills okända virus och andra typer av infektioner.
De åtgärder som vidtas anses effektiva mot höljeförsedda virus såsom humant immunbrist virus (HIV), hepatit B virus (HBV) och hepatit C virus (HCV) och för det icke-höljeförsedda viruset hepatit A (HAV). Åtgärderna kan vara av begränsat värde mot icke-höljeförsedda virus som parvovirus B19. Parvovirus B19-infektion kan vara allvarlig för gravida kvinnor (infektion av fostret) och för individer med nedsatt immunförsvar eller har någon slag anemi (t.ex. sickelcell sjukdom eller onormal nedbrytning av röda blodkroppar).
Andra läkemedel och Octafil Low
Tala om för läkare eller apotekspersonal om du använder, nyligen har använt eller kan tänkas använda andra läkemedel, inklusive sådana som är receptfria.
Inga kända interaktioner finns mellan produkter som innehåller koagulationsfaktor VIII från humant blod och andra läkemedel. Octafil Low ska ändå inte kombineras med andra läkemedel under infusionen.
Graviditet och amning
Rådfråga läkare eller apotekspersonal innan du använder något läkemedel.
Körförmåga och användning av maskiner
Inga effekter har observerats på förmågan att framföra fordon och använda maskiner.
Octafil Low innehåller natrium
Detta läkemedel innehåller upp till 40 mg natrium (huvudingrediensen i koksalt/bordssalt) per injektionsflaska. Detta motsvarar 2 % av högsta rekommenderat dagligt intag av natrium för vuxna.
3. Hur produkten används
Octafil Low ska ges intravenöst efter rekonstituering med den medföljande vätskan.
Behandling ska påbörjas under övervakning av läkare.
Dosering för att förhindra blödning
Om du har svår hemofili A ska du injicera 20 till 40 IE faktor VIII per kg kroppsvikt varannan eller var tredje dag för förebyggande långtidsbehandling. Doseringen ska justeras efter ditt svar. I vissa fall kan kortare doseringsintervall eller högre doser krävas.
Dosberäkning
Använd alltid Octafil Low exakt så som din läkare har sagt. Kontrollera med din läkare eller apotekspersonal om du är osäker.
Faktor VIII-aktivitet avser mängden faktor VIII i plasma. Den uttrycks antingen som andel i procent (i förhållande till normal human blodplasma) eller i internationella enheter (IE). Dosen av faktor VIII uttrycks i IE.
En IE faktor VIII-aktivitet motsvarar mängden faktor VIII i en ml normal human blodplasma. En IE faktor VIII per kg kroppsvikt höjer faktor VIII-aktiviteten i plasma med 1,5% - 2% av normal aktivitet. För att beräkna dosen mäts nivån av faktor VIII-aktivitet i din blodplasma. Denna visar hur mycket aktiviteten behöver höjas. Rådgör med din läkare om du är osäker på hur mycket din faktor VIII-aktivitet behöver höjas eller hur du ska beräkna dosen.
Erforderlig dos beräknas med hjälp av följande formel:
Erforderliga enheter = kroppsvikt (kg) x önskad ökning av faktor VIII (%)
(IE/dl) x 0,5 |
Dosens storlek och hur ofta den ska ges (frekvens) ska alltid vägledas av den kliniska effekten hos den enskilda patienten.
Vid följande blödningshändelser ska faktor VIII-aktiviteten inte sjunka under den aktivitetsnivå i plasma (i % av normal aktivitet) som anges i nedanstående tabell för motsvarande period. Tabellen kan användas för vägledning avseende dosering vid blödning och kirurgiska ingrepp:
Grad av blödning / Typ av kirurgiskt ingrepp | Erforderlig faktor VIII-nivå (%) (IE/dl) | Doseringsfrekvens (timmar mellan dosering) / Behandlingens längd (dagar) |
| Blödning | | |
| Blödning in i en led (tidig hemartros), muskelblödning eller blödning i munnen | 20–40 | Upprepa en till två ggr per dygn i minst ett dygn, till dess smärtan avtar eller läkning uppnås. |
| Mer omfattande blödning in i en led (hemartros), muskelblödning eller blodutgjutning (hematom) | 30–60 | Upprepa infusionen en till två ggr per dygn i 3-4 dagar eller mer, till dess smärta och funktionsnedsättning har upphört. |
| Livshotande blödning, t.ex. vid kirurgiska ingrepp i huvudet, blödning i halsen, kraftig blödning i buken | 60–100 | Upprepa infusionen var 8:e timme eller en gång per dygn till dess hotet är avvärjt. |
| Kirurgi | | |
| Mindre ingrepp inkl. tandutdragning | 30–60 | En gång per dygn i minst ett dygn tills läkning uppnås. |
| Större ingrepp | 80–100 (före och efter operation) | Upprepa infusionen var 8:e timme eller en gång per dygn till dess god sårläkning erhålls. Behandla därefter i ytterligare minst 7 dagar för att hålla faktor VIII-aktiviteten på 30% till 60%. |
Din läkare anger i vilken dos och hur ofta du ska använda Octafil Low.
Ditt svar på behandling med faktor VIII-produkter kan variera. Faktor VIII-nivån i ditt blod ska därför mätas under behandlingen för att beräkna rätt dos och infusionsfrekvens.
Användning för barn
Kliniska studier visade inte på några specifika doseringsbehov för barn. Dosering till barn och vuxna är densamma, både för behandling och för profylax.Instruktioner för hemvård
- Läs noga igenom alla anvisningar och följ dem noggrant!
- Använd inte Octafil Low efter utgångsdatumet som står på etiketten.
- Sterilitet måste upprätthållas under proceduren som beskrivs nedan.
Berett läkemedel ska inspekteras visuellt med avseende på partiklar och missfärgning före administreringLösningen i sprutan skall vara klar eller svagt opaliserande (mjölkig). Använd inte lösningen om den är grumlig eller har fällning.Använd den rekonstituerade lösningen omedelbart för att undvika mikrobiell kontamination.Använd enbart det medföljande infusionshjälpmedel. Används andra injektions/infusionsredskap så kan det öka risken och förorsaka misslyckad behandling.Anvisningar för färdigberedning av lösningen
Anvisningar för beredning av Octafil Low lösning (rekonstituering):
- Använd inte produkten direkt när den tagits ur kylskåpet. Låt vätskan för injektionsvätska och pulvret i de oöppnade flaskorna uppnå rumstemperatur.
- Ta bort kapsylerna från både flaskorna med pulver och vätska och rengör gummipropparna med desinfektionstork som medföljer.
Överföringssetet avbildas i bild 1. Placera injektionsflaskan med spädningsvätska på en plan yta och håll den stadigt. Ta överföringssetet och vänd den upp och ned. Sätt den blå delen av överföringssetet på flaskan med spädningsvätska och tryck bestämt tills det klickar (bild 2+3). Vrid inte medan du ansluter.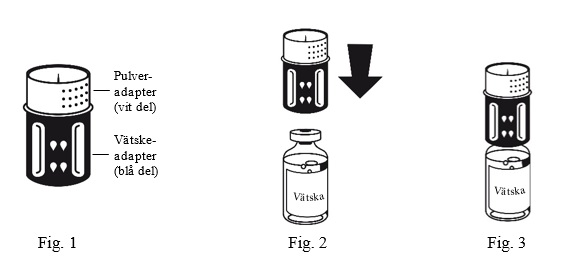
4. Placera injektionsflaskan med pulvret på en plan yta och håll den stadigt. Ta injektionsflaskan med spädningsvätska med det anslutna överföringssetet och vänd den upp och ned. Sätt den vita delen på pulverflaskans propp och tryck bestämt tills det klickar (Fig.4). Vrid inte medan du ansluter. Vätskan rinner automatiskt över till pulverflaskan.
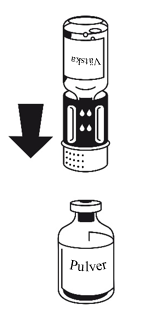
5. Rotera pulverflaskan långsamt med båda flaskorna anslutna tills pulvret löst sig. Pulvret löser sig på mindre än 10 minuter vid rumstemperatur. Lätt skumbildning kan förekomma under upplösningen. Skruva isär överföringssetet i två delar (bild 5). Då försvinner skummet.
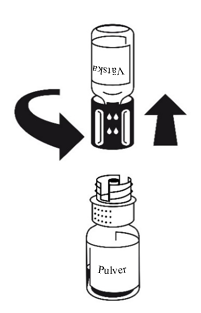
Kassera vätskeflaskan med den blå delen av överföringssetet fastsatt.Anvisningar för injektion:
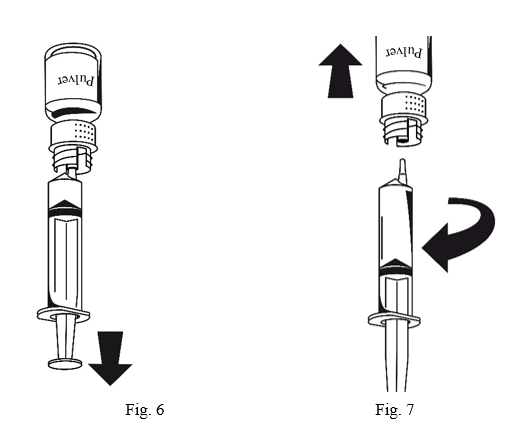
Som en försiktighetsåtgärd ska din puls tas före och under injektionen. Om pulsen stiger markant ska injektionshastigheten minskas eller administrationen tillfälligt avbrytas.1. Anslut sprutan till den vita delen av överföringssetet. Vänd flaskan upp och ned och drag upp lösningen i sprutan (bild 6).
Lösningen ska vara klar eller svagt opaliserande.
När lösningen har överförts, håll stadigt i sprutans kolv (med kolven nedåt) och avlägsna sprutan från överföringssetet (bild 7).Kassera den tomma flaskan tillsammans med den vita delen av överföringssetet.
2. Rengör det valda injektionsstället med en av de bipackade desinfektionstorkarna.
3. Anslut det bipackade infusionssetet till sprutan.
4. Stick in injektionsnålen i den valda venen. Om du har använt stasband för att lättare se venen, bör detta öppnas innan du påbörjar injektionen,
5. Blod får inte komma in i sprutan på grund av risken för koagelbildning.
6. Injicera lösningen långsamt i venen, ej mer än 2-3 ml per minut.
Om du använder mer än en flaska Octafil Low pulver vid samma behandlingstillfälle kan samma infusionsset och spruta användas. Överföringssetet är endast för engångsbruk.
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.Om du har använt för stor mängd av Octafil Low
Inga symtom på överdosering med human koagulationsfaktor VIII har rapporterats. Rekommenderad dos ska dock inte överskridas.
Om du har glömt att ta Octafil Low
Ta inte dubbel dos för att kompensera för glömd dos. Fortsätt omgående med nästa dos, och fortsätt enligt råd från läkare eller apotekspersonal.
Om du har ytterligare frågor om detta läkemedel, kontakta läkare eller apotekspersonal.
4. Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Överkänslighet eller allergiska reaktioner är sällsynta (förekommer hos1 till 10 användare av 10 000 patienter) men har iakttagits hos patienter som behandlas med produkter som innehåller faktor VIII.
Kontakta din doktor om du får följande symtom:
Tidiga tecken på allergiska reaktioner kan inkludera: illamående (kräkningar), brännande och stickande känsla på infusionsstället, trånghetskänsla i bröstet, hjärtklappning (takykardi), frossbrytningar, sjukdomskänsla, känsla av att det ”kryper i kroppen”, hudrodnad, huvudvärk, nässelutslag (urtikaria), lågt blodtryck (hypotoni), utslag, rastlöshet, svullnad i ansikte, läppar, mun, tunga eller svalg som kan orsaka svårigheter att svälja eller andas (angioödem), trötthet (letargi), väsande andning.
I mycket sällsynta (förekommer hos färre än 1 användare av 10 000) fall kan denna överkänslighet leda till en allvarlig reaktion som kallas anafylaxi och som kan inkludera chock liksom vissa av de symtom som beskrivs ovan. Om detta skulle inträffa ska du omedelbart informera din doktor eller ringa efter ambulans.
Andra sällsynta biverkningar (förekommer hos 1 till 10 användare av 10 000 patienter)
Feber
Bland barn som inte behandlats med faktor VIII-läkemedel tidigare är det mycket vanligt att hämmande antikroppar utvecklas (se avsnitt Vad du behöver veta innan produkten används) (förekommer hos fler än 1 av 10 patienter). För patienter som tidigare har behandlats med faktor VIII (behandling mer än 150 dagar) är dock risken mindre och komplikationen är mindre vanlig (förekommer hos färre än 1 av 100 användare). Om du eller ditt barn utvecklar antikroppar kan läkemedlen upphöra att fungera som de ska, och du eller ditt barn kan drabbas av ihållande blödningar. Om detta händer ska du omedelbart kontakta läkare.
För information om virussäkerhet, se Vad du behöver veta innan produkten används. (Information om blod och plasma som används för framställning av Octafil Low).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt via det nationella rapporteringssystemet (se detaljer nedan). Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet.
webbplats: www.fimea.fi
Säkerhets- och utvecklingscentret för läkemedelsområdet Fimea
Biverkningsregistret
PB 55
FI-00034 Fimea
5. Hur produkten ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på etiketten. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras i kylskåp (2–8 °C).
Får ej frysas.
Förvaras i originalförpackningen. Ljuskänsligt.
Upplöst produkt ska användas omedelbart och vid endast ett tillfälle.
Använd inte detta läkemedel om du märker att det är grumligt eller där pulvret inte har lösts helt.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
6. Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
Den aktiva substansen är koagulationsfaktor VIII från humant blod.
Volym och koncentration
Octafil Low injektionsflaska (IE faktor VIII) | Lösningsmedel (löses upp till Octafil Low pulver) (ml) | Nominell koncentration av färdigberedd lösning (IE faktor VIII/ml) |
| 1000 IE | 5 ml | 200 IE/ml |
Övriga innehållsämnen i pulvret är natriumcitrat, natriumklorid, kalciumklorid och glycin. Lösningsmedel: vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
Octafil Low levereras som pulver och vätska för injektionsvätska för lösning.
Ett vitt eller ljusgult pulver eller spröd massa.
Vätskan är klar och färglös vätska.
Den tillgängliga förpackningen innehåller humkan koagulationsfaktor VIII och vätska:
200 IU/ml pulver och vätska:
- Pulver, 1000 IE, i en injektionsflaska med propp och kapsyl.
- 5 ml vätska i en injektionsflaska med propp och kapsyl.
- 1 förpackning med utrustning för intravenös injektion (1 överföringsset, 1 infusionsset, 1 engångsspruta)
- 2 desinfektionstorkar.
Alla förpackningsstorlekar kommer eventuellt inte att marknadsföras.
Innehavare av godkännande för försäljning
Octapharma AB
Lars Forssells gata 23
SE-112 75 Stockholm
Sverige
Tillverkare
Octapharma Pharmazeutika Produktionsges.m.b.H.
Oberlaaerstr. 235
A-1100 Wien
Österrike
eller
Octapharma S.A.S
70-72 Rue du Maréchal Foch
BP 33, F-67381 Lingolsheim
Frankrike
eller
Octapharma AB
Lars Forssells gata 23
SE-112 75 Stockholm
Sverige
Detta läkemedel är godkänt i det europeiska ekonomiska samarbetsområdet under följande namn:
Octanate LV: Cypern, Danmark, Frankrike, Holland, Malta, Polen, Rumänien, Spanien, Storbritannien, Sverige, Österrike
Octafil Low: Finland
Octanate: Belgien, Tjeckien, Tyskland, Irland, Italien, Lettland, Litauen, Luxemburg, Portugal
Octanate Kons: Slovenien
Denna bipacksedel ändrades senast 20.11.2023.